Un cerveau tout neuf, sorti du laboratoire
Un chercheur genevois escompte reconstruire des parties manquantes du cortex cérébral. Il a déjà développé le matériel nécessaire. Mais la technique se heurte encore à des obstacles majeurs et soulève beaucoup de scepticisme.
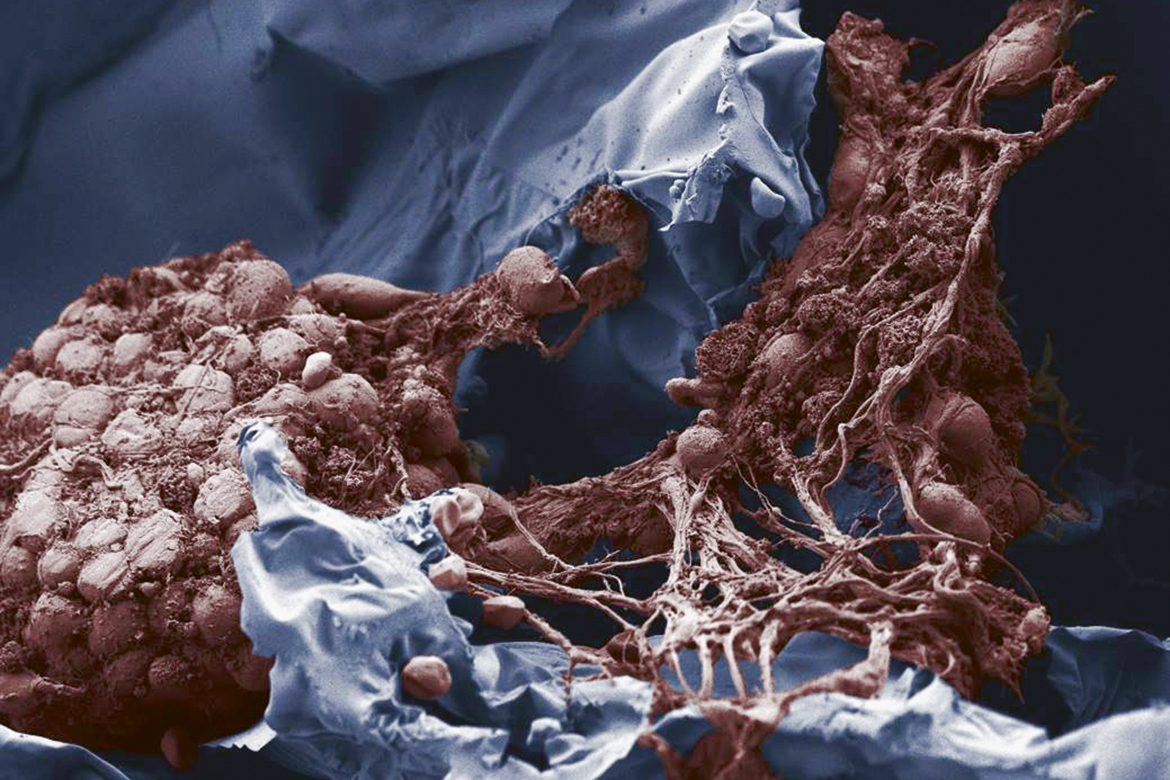
Le gel (en bleu) protège les cellules nerveuses (en brun) lors de l’implantation. Prise de vue teinte au microscope électronique. | Photo: Aleksandra Filippova
Les cellules du cerveau détruites lors d’un accident vasculaire cérébral, par le Parkinson et d’autres maladies neurodégénératives, sont perdues à jamais. On ne peut simplement combler les vides laissés. C’est pourtant l’ambition de Thomas Braschler, spécialiste en matériaux à l’Université de Genève, qui a développé une nouvelle forme de gel à injecter sous forme de filaments dans les zones lésées du cerveau. Cette bio matière est au préalable chargée de cellules nerveuses pour remplacer les tissus perdus, établir de nouvelles connexions et produire des neurotransmetteurs.
Avec son équipe, il a travaillé d’arrache-pied pendant trois ans afin de trouver le support adéquat pour transporter les cellules de remplacement dans le cerveau avec une extrême précision et sans les endommager. «C’est une gageure d’implanter des cellules nerveuses, car leurs longs axones se déchirent facilement, dit Thomas Braschler. Nous avons maintenant largement résolu ce problème.»
Les neurofilaments développés par le chercheur sont épais comme du fil à coudre et mesurent environ un demi-centimètre. A base de cellulose, le gel spongieux est produit à des températures inférieures au point de congélation. Creux, ces fils forment une structure stable pour l’implantation de cellules nerveuses. La matière, élastique et souple à la fois, peut être comprimée et pressée à travers une seringue. Les résultats des premières expériences sont encourageants: bien que fragiles, les cellules nerveuses incorporées dans ce support survivent à l’injection dans un cerveau de souris. Mieux encore: elles y restent en vie pendant au moins un mois.
Pas de contact entre les cellules
L’idée de développer un tel matériau de support n’est pas nouvelle. «Hélas, l’espoir que ces implants contribuent à reconstruire le tissu nerveux ne s’est concrétisé que dans de très rares cas à ce jour», note Martin E. Schwab, professeur de recherche sur le cerveau à l’Institut de médecine régénérative de l’Université de Zurich. Il a lui-même déjà expérimenté les matériaux les plus variés pour pallier les lésions de la moelle épinière et celles provoquées par des AVC. «Le système nerveux central n’intègre les implants qu’à grand-peine et très mal.» Les inflammations sont donc fréquentes, entraînant la résorption ou l’encapsulation du matériau intrus.
Thomas Braschler admet que de tels effets indésirables doivent dans tous les cas être clarifiés dans le cadre d’études à large échelle. En revanche, il n’a encore observé aucune encapsulation significative dans de petites séries de tests. Quant à la résorption du matériau, elle est même souhaitable, mais seulement une fois que les cellules nerveuses se sont intégrées aux tissus environnants.
Martin E. Schwab reste sceptique pour d’autres raisons encore: «L’idée de reconstruire un morceau du cortex cérébral est très audacieuse. » Car les cellules implantées devraient non seulement survivre, mais aussi parvenir à établir des connexions judicieuses avec les cellules avoisinantes. «Quand il manque un morceau important de cortex cérébral, qui commande par exemple un bras ou le langage, il ne suffit pas d’injecter quelques millions de cellules, car elles ignorent ce qu’elles doivent faire.»
Traitement spécial pour transformer des cellules souches embryonnaires
Thomas Braschler n’a en effet pas encore pu démontrer que les cellules nerveuses injectées entraient bel et bien en contact avec leurs voisines. Les premières expériences dans ce sens sont déjà en cours. Thomas Braschler suit aussi des voies inédites dans le choix des cellules nerveuses transplantées: par un traitement spécial, il transforme des cellules souches embryonnaires en cellules nerveuses à maturité, produisant de la dopamine, et cela directement dans les neurofilaments. Il croit qu’implanter de telles cellules pourrait aider en particulier les patients atteints de la maladie de Parkinson. Car une carence en dopamine dans le cerveau entraîne les troubles moteurs et autres symptômes typiques de cette affection.
Hans Rudolf Widmer, expert de cette maladie, juge l’idée plutôt bonne. Le professeur de neurosciences dirige le laboratoire de recherche de la clinique universitaire de neurochirurgie de l’Hôpital de l’Ile à Berne. Il planche depuis plus de vingt -cinq ans sur la possibilité de traiter le Parkinson en transplantant des cellules cérébrales. Bien que prometteuses, ces approches sont encore loin d’une application sur les patients et s’accompagnent de nombreuses difficultés: beaucoup de chercheurs transplantent des cellules souches embryonnaires, alors qu’elles risquent de se multiplier de façon incontrôlée et de former des tumeurs.
«Thomas Braschler contourne ce problème par l’emploi de cellules nerveuses adultes. Mais il en résulte un autre, de taille, à savoir que le système immunitaire les rejette», note Hans Rudolf Widmer. Il rappelle que son confrère n’a encore mené ses expériences que sur des souris immunodéprimées, qui ne peuvent faire de rejet.
Mais le chercheur genevois envisage déjà une solution: d’après les premiers tests, les propres cellules du corps ne sont pas rejetées dans son procédé. Actuellement, de nombreux groupes de recherche tentent d’en produire pour obtenir des cellules nerveuses fabriquant de la dopamine à partir de celles du patient plutôt qu’à partir de cellules souches embryonnaires. Ainsi, toute réaction immunitaire est impossible.
Des résultats très provisoires encore
Le professeur Widmer juge les résultats de Thomas Braschler encore très provisoires, entre autres parce qu’il n’a pas pu prouver que les cellules nerveuses formaient des ramifications dans le cerveau. De plus, les neurofilaments n’ont pas encore été testés sur des souris spéciales qui simulent la maladie de Parkinson. Le professeur estime néanmoins que la recherche de thérapies novatrices contre le Parkinson est une bonne idée: «La maladie est incurable et touche beaucoup de gens. Les seuls traitements disponibles induisent souvent de graves effets secondaires au fil des ans.»
Thomas Braschler sait bien que beaucoup jugent son concept utopique: «Mais l’important est d’aspirer à quelque chose. Tout résultat permet de suivre d’autres pistes prometteuses.» Une start-up biotech est ainsi née de l’idée d’utiliser son gel à d’autres fins médicales, comme de remplacer des tissus adipeux et conjonctifs perdus lors de l’ablation de tumeurs. «C’est comme avec l’étoile polaire. Même en la suivant, on ne l’atteindra jamais. Pourtant, elle guide nos pas dans la bonne direction.»

Le spécialiste en matériaux Thomas Braschler sait bien que beaucoup jugent son idée utopique. | Photo: Daniel Rihs